Wir sind am 01.04. umgezogen! Unsere neue Adresse ist: Reimerstwiete 11, 20457 Hamburg
Ein erfolgreicher Arzneimittel-Launch steht und fällt mit guter Planung. Neben klinischen, regulatorischen und logistischen Themen spielt auch die Kommunikationsstrategie eine zentrale Rolle. Denn ein verzögerter Start einer Launch-Kampagne, unklare Zuständigkeiten oder nicht sauber abgestimmte Freigaben können wertvolles Marktpotenzial und damit Umsatz kosten. Wer jedoch Anforderungen und Timelines kennt und frühzeitig die nötigen Vorbereitungen trifft, schafft die Grundlage für einen erfolgreichen Launch.
Für alle Launch Aktivitäten im Pharma-Marketing gelten klare regulatorische Vorgaben. Grundsätzlich dürfen Arzneimittel erst nach erteilter Zulassung beworben werden. Dies ist unter anderem in der Richtlinie 2001/83/EG Art. 87 (1) sowie in § 3a HWG (DE) und § 50a (1) AMG (AT) geregelt. Zudem ist die Ansprache bei verschreibungspflichtigen Präparaten ausschließlich auf Fachkreise beschränkt (§ 10 HWG (DE), § 54 AMG (AT)).
Für den Launch bedeutet das: Marketingmaterialien und Kampagnen können zwar vor der Zulassung vorbereitet werden, dürfen jedoch erst ab dem Zeitpunkt der Zulassung kommuniziert werden. Die rechtlichen Rahmenbedingungen sollten unbedingt eingehalten werden. Andernfalls drohen Abmahnungen, die die gesamte Launch Strategie gefährden und im schlimmsten Fall zu Verzögerungen oder sogar zum Stopp geplanter Marketingaktivitäten führen können.
Für einen erfolgreichen und reibungslosen Launch ist es entscheidend, frühzeitig eine klare Marketingstrategie zu entwickeln, die auf fundierten Marktanalysen, einer präzisen Zielgruppendefinition und einer überzeugenden Positionierung basiert. Der medizinische Mehrwert des Produkts muss klar herausgearbeitet und in eine konsistente Kommunikationsstrategie übersetzt werden, wobei auch Marktanalysen stets im Einklang mit den Vorgaben des HWG stehen müssen.
Wichtig ist, dass während der Launch-Phase alle Aktivitäten auf ein gemeinsames Ziel ausgerichtet sind. Unternehmen sollten relevante KOLs identifizieren sowie zentrale Botschaften frühzeitig definieren und vor allem an Mitarbeitende kommunizieren. Unterstützt durch Marktforschung, klare KPIs und eine strukturierte Datenstrategie entsteht so die Grundlage, um Maßnahmen effektiv zu steuern und den Markteintritt erfolgreich zu gestalten.
Neben der strategischen Vorbereitung bietet die Phase vor der Zulassung die Möglichkeit bereits frühzeitig Kommunikationsmaßnahmen umzusetzen. Zwar ist Produktwerbung noch nicht zulässig, jedoch bieten insbesondere Disease-Awareness-Kampagnen die Möglichkeit über Erkrankungen zu informieren und sich bereits thematisch im Markt zu positionieren. Als etabliertes Instrument können sie dazu beitragen, Versorgungslücken sichtbar zu machen, Diagnostikpfade zu erläutern und Therapieziele einzuordnen. Inhalte sollten dabei stets medizinisch ausgewogen, evidenzbasiert und transparent sein, ohne überzogene Erwartungen zu wecken oder gegenüber den Adressenten Angst zu schüren.
Entscheidend bei einer Disease-Awareness-Kampagne ist die klare Abgrenzung zur Produktkommunikation: Der Fokus muss konsequent auf der Erkrankung liegen. Denn rechtlich gilt ein strenger Maßstab. Nach der Rechtsprechung des EuGH kommt es für die Einordnung als Werbung entscheidend darauf an, ob eine Maßnahme der Absatzförderung dient (EuGH, Urteil vom 05.05.2011 – C-316/09). Somit können auch Inhalte ohne direkten Produktbezug als Werbung eingeordnet werden. Gerade im Vorfeld einer Zulassung ist daher besondere Vorsicht geboten, um unzulässige Arzneimittelwerbung zu vermeiden. Zuspitzend könnte man sagen: „je näher die Kommunikation einer Firma zeitlich am Launch liegt, desto größer ist die Wahrscheinlichkeit, dass sie als Werbung i.S.d. HWG interpretiert wird“.
Wer als pharmazeutischer Unternehmer Fertigarzneimittel in Deutschland oder Österreich in den Verkehr bringt, muss gemäß § 74a Abs. 1 AMG (DE) bzw. § 56 (2) AMG (AT) einen Informationsbeauftragten (IB) benennen, der die Kommunikation rund um das zugelassene Arzneimittel verantwortet. In der Praxis bedeutet dies, dass Kommunikationsmaterialien durch den IB freigegeben werden müssen.
Obwohl der IB erst ab der Zulassung des Arzneimittels Materialien freigeben muss, ist es sinnvoll ihn bereits einige Monate vorher zu benennen. So kann er frühzeitig in seine Rolle eingearbeitet werden, notwendige Zugänge erhalten und sich mit Prozessen und Materialien vertraut machen.
Ein zusätzlicher Vorteil: Marketingmaterialien können bereits vorab einem Pre-Review unterzogen werden. Da zum Launch erfahrungsgemäß eine Vielzahl an Freigaben gleichzeitig anfällt, ermöglicht ein Pre-Review eine deutlich schnellere finale Freigabe.
Der Pflichttext gemäß § 4 HWG kann im Launch-Prozess schnell zum Engpass werden. Während Marketingmaterialien meist bereits vor der Zulassung erstellt werden, liegt der Pflichttext zu diesem Zeitpunkt oft noch nicht vor. Nach der Zulassung muss dieser dann erst erstellt, geprüft und in alle werblichen Materialien integriert werden. Dies kann den Kampagnenstart verzögern.
Um den Prozess schneller zu gestalten, empfiehlt es sich, den Pflichttext frühzeitig „at risk“ auf Basis der vorläufigen Fachinformation (SmPC) zu erstellen und bereits in Marketingmaterialien einzuarbeiten. Da sich die Inhalte häufig nicht mehr wesentlich ändern, kann die finale Version nach der Zulassung in der Regel schnell geprüft und freigegeben werden. So lässt sich wertvolle Zeit sparen und ein reibungsloser Launch sicherstellen.
Ein erfolgreicher Launch erfordert nicht nur gute Marketingmaterialien, sondern auch klare interne Prozesse im Hintergrund. Unternehmen sollten daher Prozesse für die Prüfung und Freigabe von werblichen und nicht-werblichen Materialien implementieren und diese in SOPs festhalten. Darin sollten Verantwortlichkeiten, Review-Prozesse und Freigabekriterien festgelegt werden.
Ebenso wichtig ist die Schulung aller relevanten Mitarbeitenden. Neben Trainings der internen SOPs, sollten auch Launch-Strategien und Compliance Themen frühzeitig vermittelt werden. Nur so wird sichergestellt, dass Launch Strategien effizient und compliant umgesetzt werden und interne Prozesse reibungslos ablaufen.
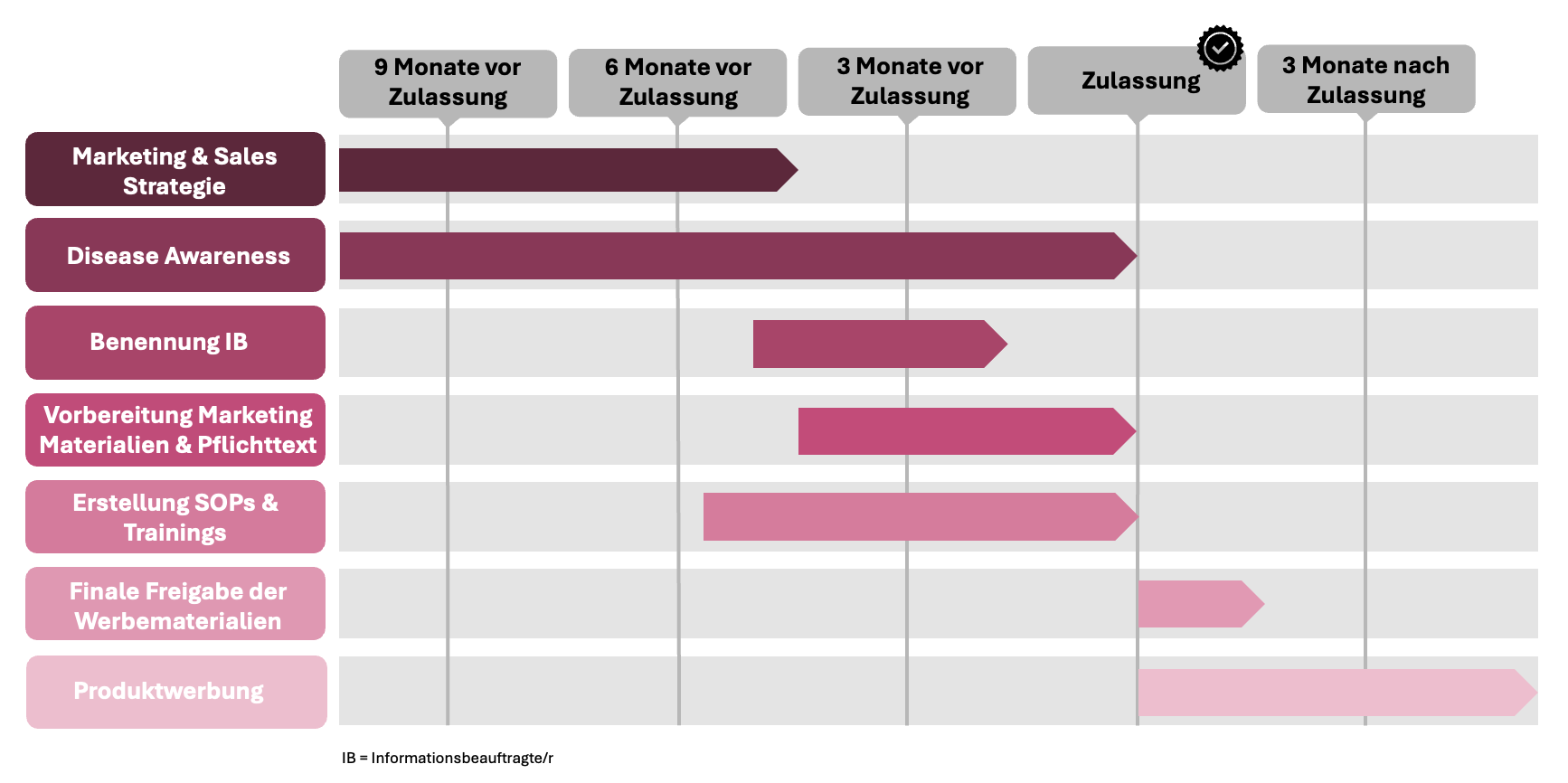
Der Erfolg eines Arzneimittel-Launches wird maßgeblich in der Phase vor dem Markteintritt entschieden. Entscheidend ist, wie gut Strategie, regulatorische Anforderungen und operative Prozesse vorbereitet und umgesetzt werden. Eine fehlende Launch-Strategie, unklare Zuständigkeiten oder fehlende Abstimmung können dabei schnell zum Risiko für den gesamten Launch werden und damit den Erfolg eines Arzneimittels entscheidend beeinflussen.
In der Praxis hat sich bei uns die Nutzung einer Launch-Checkliste bewährt, mit der wir Unternehmen dabei unterstützen, alle relevanten Schritte strukturiert zu erfassen, Engpässe frühzeitig zu erkennen und den Launch gezielt vorzubereiten. Das schafft Transparenz, erhöht die Umsetzungssicherheit und legt die gemeinsame Grundlage für einen erfolgreichen Launch.